氢氧燃料电池的原理
料电池是一种化学电池,它运用物质发作化学反响时释出的能量,直接将其变换为电能。从这一点看,它和其他化学电池如锰干电池、铅蓄电池等是相似的。可是,它作业时需求接连地向其供应反响物质——燃料和氧化剂,这又和其他一般化学电池不大一样。因为它是把燃料经过化学反响释出的能量变为电能输出,所以被称为燃料电池。
具体地说,燃料电池是运用水的电解的逆反响的”发电机”。它由正极、负极和夹在正负极中心的电解质板所组成。开始,电解质板是运用电解质进入多孔的板而构成,现在正发展为直接运用固体的电解质。
作业时向负极供应燃料(氢),向正极供应氧化剂(空气)。氢在负极分解成正离子H+和电子e-。氢离子进入电解液中,而电子则沿外部电路移向正极。用电的负载就接在外部电路中。在正极上,空气中的氧同电解液中的氢离子吸收抵达正极上的电子构成水。这正是水的电解反响的逆进程。
运用这个原理,燃料电池便可在作业时源源不断地向外部输电,所以也可称它为一种”发电机”。
一般来讲,书写燃料电池的化学反响方程式,需求高度留意电解质的酸碱性。 在正、负极上发作的电极反响不是孤立的,它往往与电解质溶液紧密联系。如氢—氧燃料电池有酸式和碱式两种,在酸溶液中负极反响式为:2H2-4e-==4H+ 正极反响式为:O2+4H++4e-==2H2O;如是在碱溶液中,则不可能有H+呈现,在酸溶液中,也不可能呈现OH-。根据电解质的不同,燃料电池(Fuel Cell, FC)分为碱性燃料电池(AFC)、磷酸型燃料电池(PAFC)、熔融碳酸盐燃料电池(MCFC)、固体氧化物燃料电池(SOFC)及质子交流膜燃料电池(PEMFC)等。其间归于碱性燃料电池的只要AFC一种,而其他的燃料电池均归于酸性燃料电池,不存在所谓的中性燃料电池,只要电解质为弱酸或弱碱而挨近中性的燃料电池。
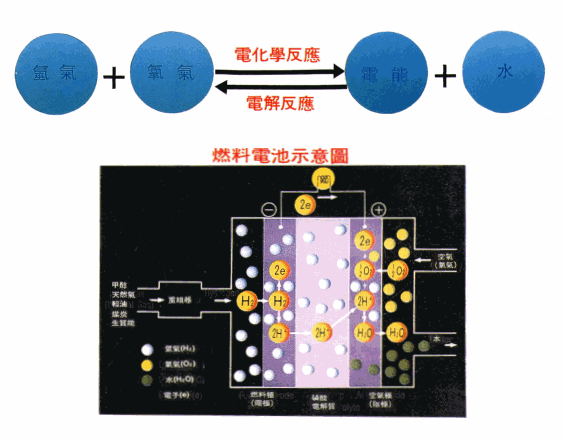
燃料电池的电极反响式与其电解质的酸碱性紧密联系。
当电解质溶液挨近中性时:
负极:2H2-4e=4H+ 正极:O2+4e+2H2O=4OH-
当电解质溶液呈酸性时:
负极:2H2-4e=4H+ 正极:O2+4e+4H+=2H2O
当电解质溶液呈碱性时:
负极:2H2-4e+4OH-=4H2O 正极:O2+4e+2H2O=4OH-
留意一切的电子e都省掉了负号上标,书写时应当加上。