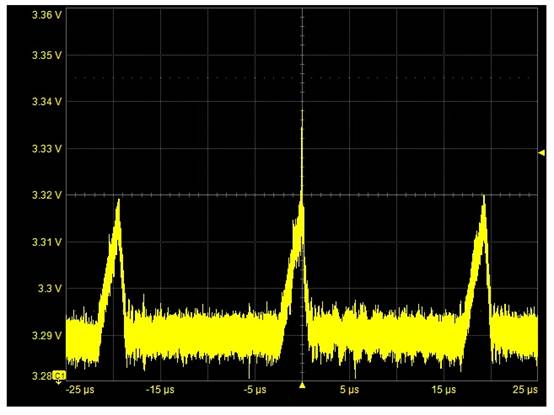
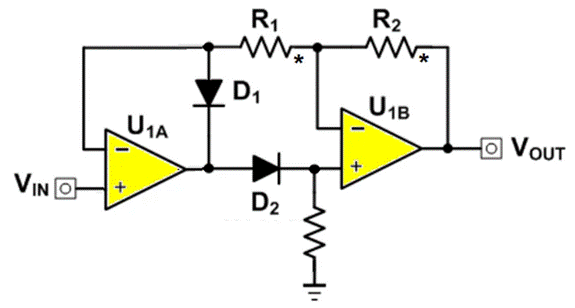
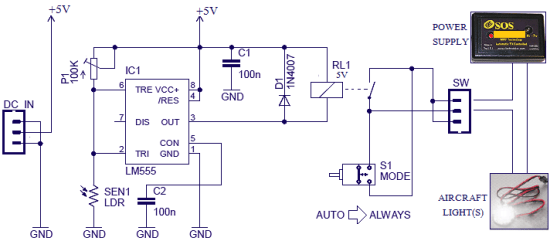
为进步临床实验数据的质量,CFDA最近推出对已申报的临床药物数据的进行自查核对。咱们了解自查核对分2个方面 (图1),一是对药物本身,另一是对临床中心进行自查核对。对药物的要确保有用性及安全性。对临床中心,尤其是参加性,入组率有反常及临床组长地点的临床中心进行额定查看:参加性包含挑选成功率和实验掉落率高于惯例,入组率包含入组速度及人数超凡。
本文要描绘的是用临床药物计算中的依据危险的监查来比较安全性、参加性和入组规则来剖析入组速度及人数。一起能够重视临床组长地点的临床中心,查询其安全性,参加性和入组率是否反常。别的,因为各个药物的有用性的检测办法各有不同,在此文中就不做评论。
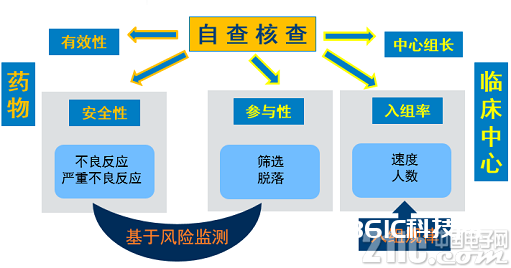
图1. 药物和临床中心的自查核对
依据危险的监查(RBM: Risk-Based Monitoring)以中心化和非现场的办法全体全面的监查重要的临床研讨目标, 然后用相应的现场监查去支撑临床中心的操作, 受试者的安全和数据的质量。其主旨是及时发现临床中心具体问题, 进步功率,降低成本。依据危险的监查一经提出,遭到业界各方,尤其是药厂的支撑和运用。
RBM有3个部分组成 (图2) 。榜首部分是是要设置危险目标,包含安全性,数据质量, 挑选,入组,掉落,研讨人员,中心Facilities和供应及有必要的文件。各个目标将危险分为3档,并以3种颜色来代表:低(绿),中(黄),高(红)。本文以CDISC标准化的数据为例,所需目标在CDISC的不同的域中, 如:不良反应 (AE: Adverse Event), 人口学 (DM Demographics), 处置(DS Disposition),受试者拜访 (SV: Subject Visits),露出(EX: Exposure), 计划违背 ,(PD: Protocol Deviations),未达标的包含/不包含的阈值 (Inclusion/Exclusion Criterion Not Met)and ADSL。 因为低,中,高3种危险是以绿,黄,红来表明,其点评成果就称为交通红绿灯体系。危险的成果可在表格顶用3色表明 (图4),地图中显现 (图5-10)及分布图来表达 (图11)。依据危险的监查可运用业界认可惯例目标的危险阈值,一起,也答应研讨者依据临床实验的具体状况自定义额定的危险目标,及对惯例危险目标和新增的危险目标的阈值进行调整。
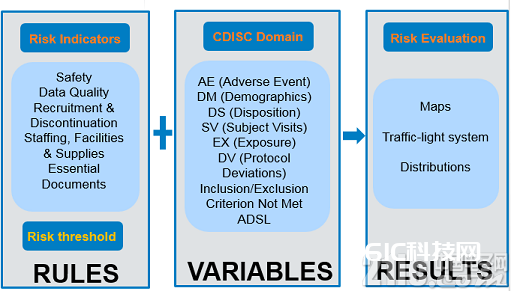
图2. RBM的3个首要部分
依据危险的监查显现一系列的危险目标 (图3)。 其间对不良反应,严峻不良反应是CFDA所要求的安全性的监查,挑选成功率和实验掉落率也是依据危险的监查的惯例监查目标。依据危险的监查除了有单项危险目标,还通过计算模型取得归纳危险目标。
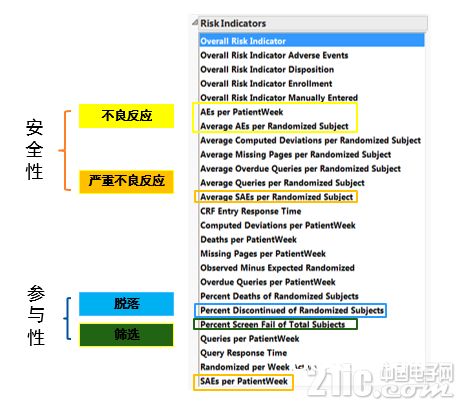
图3.依据危险的监查一系列的危险目标
依据危险的监查的成果可用交通红绿灯体系来显现或以国家为单位(图4)或以各个临床中心为单位(图5)的归纳危险目标。
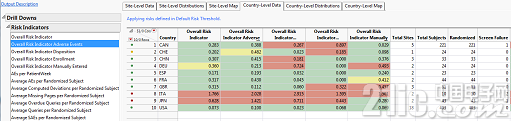
图4.以交通红绿灯体系来显现的以国家为单位的依据危险的监查的成果
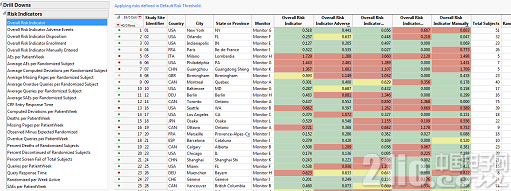
图5.以交通红绿灯体系来显现的以临床中心为单位的依据危险的监查的成果
关于各个危险目标,把危险目标的值标枳在地图上就更是一望而知了。图5是国家级的不良反应的危险目标,在这个模仿的数据中, 加拿大的不良反应是高危险,中国是中危险, 美国是低危险。图6是以临床中心为单位的严峻不良反应的危险目标,能够看出同一国家的不同临床中心的危险值是不相同的。
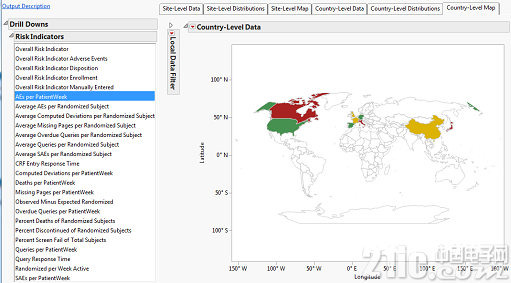
图6. 以地图来显现的以国家为单位的不良反应的危险目标
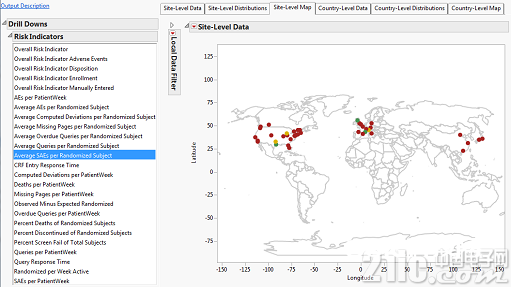
图7. 以地图来显现的以中心为单位的严峻不良反应的危险目标
相同,图8显现了在国家级的掉落率的危险和图9显现了在中心级的挑选率的危险。

图8. 以地图来显现的以国家为单位的掉落率的危险目标
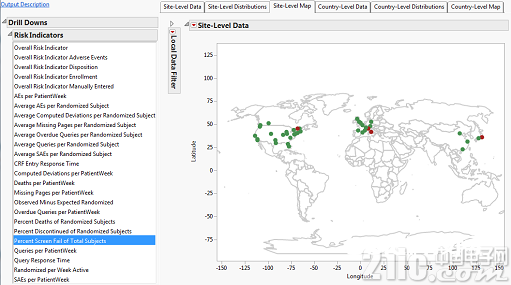
图9.以地图来显现的以中心为单位的挑选率的危险目标
归纳各项危险评价,依据危险的监查给出下一步的主张。图10中是挑选了需求重视中,高危险的临床中心。 给出的主张包含组织中心现场拜访,联络研讨主持人,评价中心资源并联络中心协调员,评价是否需求中心人员培训并联络中心协调员,长途评价数据后决议是否组织中心现场拜访; 或联络研讨主持人;或联络中心协调员。 图中在最右边的举动主张中的挑选了组织中心现场拜访, 能够看出一切需求组织中心现场拜访都是因为手动参加的危险目标其归纳危险目标归于中或高危险而形成的。

图10.依据危险的监查的举动主张
值得阐明的是在图3列出的一切归纳和个别危险目标,都能够在交通红绿灯体系及地图中显现在国家级和临床中心级的危险。
入组规则:
以中心为单位,图11显现各个临床中心在整个实验发展过程中受试者人数的增加状况。黑色的曲线是一切临床中心的平均值。其间有3个组, 第20,第28和第16临床中心的入组数量和速度都比其他的临床中心要多和快。 能够查询一下这3个组远高于平均值的原因。 一起也可了解临床组长地点的临床中心是否归于这3组之一。别的,入组特别慢而少的中心也需求了解原因。

图11. 各个临床中心在整个实验发展过程中受试者人数的增加状况
在每个中心的医治组和对照组的入组人数和速度也在图12中表明。赤色的是代表对照组,蓝色的代表医治组。这组表明该中心的医治组和对照组的入组人数和速度简直相同。

图 12. 某一中心按医治组和对照组分类的入组人数和速度
每天每个中心的入组人数在图13中显现。每个格子里代表一个临床中心。
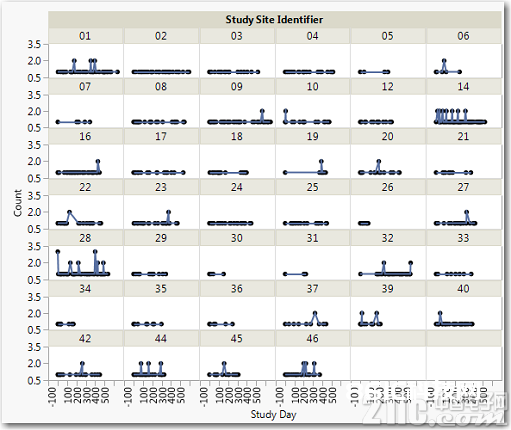
图13. 每天每个中心的入组人数
此外,期望受试者是随机入组。而不是在相邻的时刻内,只要医治组或对照组的受试者入组。图14中的最右边分布图显现333个受试者和他/她相邻入组的受试者不是来自同一医治组或对照组, 有372受试者入组时刻上是两两受试者来自同一医治组或对照组,有44个受试者的入组时刻是4个相邻入组的受试者来自同一医治组或对照组。这44个人来自对照组略多于医治组,highlight的部分显现有44个受试者, 来自9个不同的中心(深绿色部分)。

图14.受试者随机入组
计算剖析是快速判别临床实验数据的质量好坏,药物作用是否牢靠的有用东西。除了依据危险的监查外,诈骗监查也是监查数据中有意或无意的过错的有用办法。一系列的对不良反应和严峻不良反应计算办法也能够用来对其进一步的研讨。
本文一切剖析与图形与定论,都是彻底依据SAS公司下一代临床计算剖析渠道SAS JMP Clinical生成的。
关于作者:
包文俊,首席科学家,JMP生命科学部,SAS 公司,客座教授,复旦大学。